Синтез газ получение: Синтез-газ – Что такое Синтез-газ?
способы получения, производство, состав и применение
История человечества знает довольно много примеров, когда в силу необходимости рождались кардинально новые подходы к решению существующих жизненно важных проблем. Например, в Германии в промежуток между первой и второй мировыми войнами, лишенной доступа к крупным нефтяным источникам, назревал серьезный дефицит топлива, которое было необходимо для функционирования гражданской и военной техники.
Располагая существенными запасами ископаемого угля, Германия начала искать пути его трансформации в жидкое топливо, пригодное для двигателей внутреннего сгорания. Эта проблему удалось решить благодаря усилиям превосходных химиков, из которых отдельного упоминания заслуживает Франц Фишер, директор Института кайзера Вильгельма по исследованию угля.
В 1926 году Ф. Фишер и Г. Тропш опубликовали работу “О прямом синтезе нефтяных углеводородов при нормальном давлении”, где сообщалось, что при восстановлении монооксида углерода водородом при нормальном атмосферном давлении в присутствии катализаторов при температуре в 270 градусов по шкале Цельсия можно получить жидкие и твердые гомологи метана.
Так на свет появился знаменитый способ синтеза углеводородов из монооксида углерода, называемый с тех пор методом Фишера-Тропша. Благодаря данному методу смесь водорода и угарного газа в различных соотношениях может легко быть получена как из каменного угля, так и из любого другого сырья, содержащего углерод. Полученную в результате данного процесса смесь газов начали называть синтез-газом.
Состав синтез-газа
Как мы уже упомянули выше, в состав синтез-газа входят такие вещества как CO и h3. В зависимости от метода получения синтез-газа соотношение CO:Н2 в нем варьируется от 1:1 до 1:3. В прямой зависимости от применяемого сырья и метода его соотношение компонентов в синтез-газе изменяется в широких пределах. Как правило, процентное содержание веществ в сыром неочищенном синтез-газе следующее:
- CO – 15-18%
- h3 – 38-40%
- Ch5 – 9-11%
- CO2 – 30-32%
Стоит заметить, что данное соотношение является весьма приблизительным, поскольку повышением температуры в процессе синтеза можно увеличить количество СО, а увеличив давление можно повысить содержание Н2 и СН4.
Также, помимо данных веществ синтез-газ может содержать и другие вещества – инертные газы (N2) и серосодержащие соединения (h3S), если исходное сырье содержало серу. От не нужного присутствия в синтез-газе таких веществ как углекислый газ и сера избавляются путем очистки селективными растворителями.
Способы получения синтез-газа
Первым известным человечеству способом получения синтез-газа была газификация каменного угля. Данный способ был осуществлен в Англии еще в 30-е годы XIX века, и во многих странах мира до 50-х годов XX века. Впоследствии данная методика была вытеснена методами, основанными на использовании нефти и природного газа. Однако в связи с существенным сокращением мировых нефтяных ресурсов, значение процесса газификации каменного угля снова стало возрастать. К тому же, благодаря такому необходимому процессу как переработка ТБО, ученые научились добывать синтез-газ из новых, нетрадиционных источников.
Сегодня существуют три основных метода получения синтез-газа.
1. Газификация угля. Данный процесс основан на взаимодействии каменного угля с водяным паром и происходит по формуле:
C + h3O → h3 + CO.
Данная реакция является эндотермической, и равновесие при температуре 900-1000 по шкале Цельсия сдвигается вправо. Разработаны различные технологические процессы, использующие парокислородное дутье, благодаря которому наряду с упомянутой реакцией параллельно протекает экзотермическая реакция сгорания угля, которая обеспечивает необходимый тепловой баланс. Ее формула:
C + 1/2O2 → CO.
2. Конверсия метана. Данная реакция взаимодействия водяного пара и метана проводится при повышенной температуре (800-900 градусов) и давлении при присутствии никелевых катализаторов (Ni-Al2O3). Формула данного процесса:
Ch5 + h3O → CO + 3h3 .
Также в качестве сырья в данном способе вместо метана можно использовать любое сырье, содержащее углеводород.
3. Парциальное окисление углеводородов. Данный процесс, происходящий при температурах выше 1300 градусов заключается в термическом окислении углеводородов. Формула данной реакции:
Формула данной реакции:
Cnh3n + 2 + 1/2nO2 → nCO + (n + 1)h3 .
Данный способ применим к любому сырью, содержащему углеводороды но наиболее часто используется высококипящая фракция нефти – мазут.
Производство синтез-газа
Сегодня производство синтез-газа постоянно совершенствуется, поскольку востребованность данного сырья неизменно растет с каждым годом. В настоящее время учеными разрабатываются проекты подземной газификации угля, то есть планируется, что получение синтез-газа будет происходить непосредственно в пласте угля глубоко под землей. Интересен тот факт, что подобную идею уже высказывал известнейший русский ученый Д.И. Менделеев, причем более 150 лет назад.
Также благодаря современным разработкам сегодня синтез-газ научились получать газификацией не только угля и нефти, но и более нетрадиционных источников углерода, вплоть до бытовых и сельскохозяйственных отходов. Таким образом, сегодня мусороперерабатывающие заводы способны добывать такое ценное сырье как синтез газ в процессе утилизации отходов.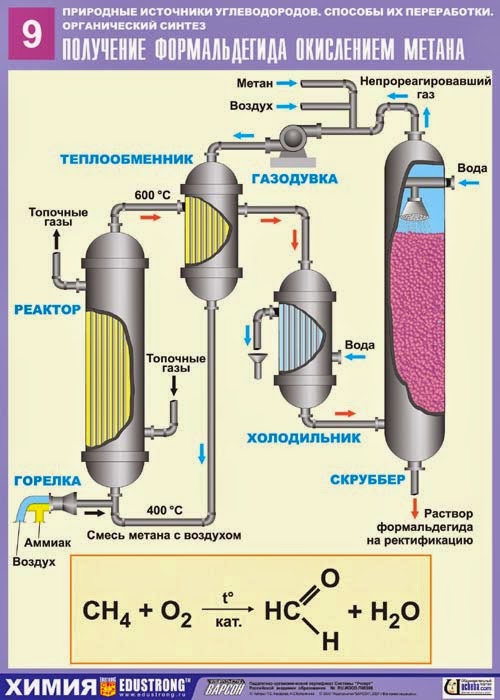
Применение синтез-газа
Сегодня синтез-газ используется в химической промышленности для получения различного сырья. Кроме этого, он также используется в качестве экологически чистого источника тепла и энергии. Сжигая синтез-газ можно получить достаточно большое количество тепла, которое можно использовать в самых различных целях.
Кроме этого, синтез газ используется в качестве исходного сырья для метилового спирта и синтетического жидкого топлива, которое по своим характеристикам ни в чем не уступает традиционному.
- Комментарии к статье
- Вконтакте
Cинтез-газ: способы получения и применение
Содержание
- 1 Определение
- 2 Получение
- 2.1 Конверсия метана с паром
- 2.2 Парциальное окисление метана
- 3 Транспортировка
- 4 Применение
- 4.1 Получение аммиака
- 4.2 Получение метанола
- 4.3 Синтез Фишера-Тропша
Определение
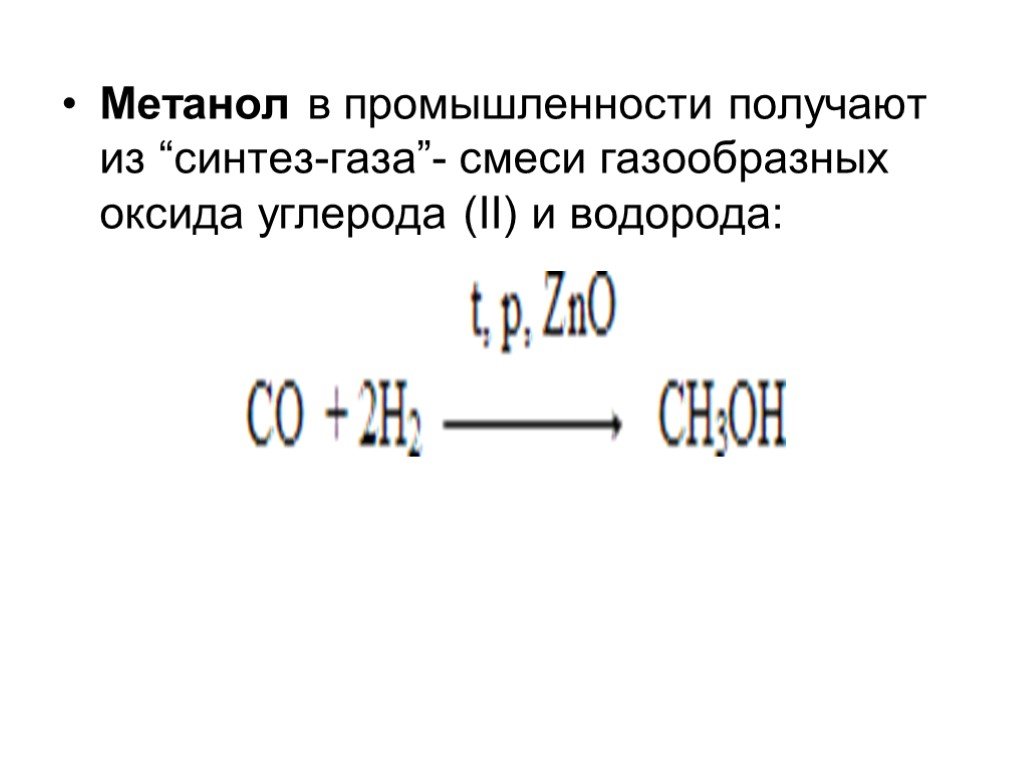
Понятие «синтез-газ» применяют к разным смесям монооксида углерода (СО) и водорода (Н2), которые используются для получения некоторых нефтехимических продуктов. Его в основном получают из природного газа (метана). Действительно, важнейшие вещества — аммиак, метанол и парафиновые углеводороды — получают именно из синтез-газа.
Его в основном получают из природного газа (метана). Действительно, важнейшие вещества — аммиак, метанол и парафиновые углеводороды — получают именно из синтез-газа.
Получение
Существуют два основных метода получения синтез-газа – конверсия метана с водяным паром и парциальное (частичное) окисление. Оба метода довольно просты.
Конверсия метана с паром
Конверсия с паром состоит в пропускании метана или нафты и водяного пара над никелевым катализатором. Реакция протекает за счет разрушительной силы высоких температур и давлений, и ее следует проводить в реакторах, аналогичных печам крекинга. При этом происходят побочные процессы, при водящие к образованию СО2 и углерода. Углерод откладывается на катализаторе и дезактивирует его.
Парциальное окисление метана
Другой метод — это парциальное (частичное) окисление метана. Процесс проводят при высоких температурах без катализатора. Метод парциального окисления обычно используют для превращения более тяжелых видов сырья — от нафты до остаточного топлива — в тех случаях, когда в распоряжении нет природного газа и легких углеводородов (этана, пропана и бутана). В обоих процессах выход суммы СО и Н2 составляет 90 – 95%.
В обоих процессах выход суммы СО и Н2 составляет 90 – 95%.
В качестве побочного продукта получают СО2, который можно удалить либо экстракцией растворителем, либо можно ввести в реакцию с водяным паром дополнительное количество метана, что даст СО и Н2. Эта реакция протекает при высоких температурах и давлениях и в присутствии никелевого катализатора.
Транспортировка
Обычно установка по производству синтез-газа бывает интегрирована в структуру завода, на котором он перерабатывается.
Единственным приемлемым способом транспортировки синтез-газа является его транспортировка по трубопроводам.
Применение
Получение и применение синтез-газаПолучение аммиака
Наиболее важной областью применения синтез-газа является производство аммиака – Nh4.
Смесь азота и водорода пропускают над железным катализатором (который содержит оксид алюминия в качестве промотора). Реакция проходит в очень жестких условиях — при температуре 420 С и давлении 280 атм.
Большая часть установок по производству аммиака снабжена оборудованием для отделения СО от сырья, так как СО может отравлять катализатор. Чаще всего с этой целью СО обрабатывают водяным паром для получения СО и Н2. Диоксид углерода удаляют экстракцией этаноламином, а Н2 направляют на рециркуляцию.
Получение метанола
Метанол часто называют древесным спиртом. Это связано с тем, что первым промышленным способом получения метанола была сухая перегонка свежеспиленной древесины лиственных деревьев. Помимо других соединений в летучей фракции присутствует метанол. Отсюда и произошло название «древесный спирт».
С 1923 г. метанол производится в промышленности из синтез-газа; в настоящее время большую часть метанола получают именно таким методом. По нескольким причинам эти установки обычно строят вблизи установок для производства аммиака или даже объединяют с ними.
Технология и оборудование аналогичны, и в производстве метанола можно использовать СО2, образующийся при синтезе аммиака. В этом случае СО2 вводят в реакцию с метаном и водяным паром над никелевым катализатором, приводящую к образованию дополнительного количества СО и Н2, которые затем взаимодействуют, давая метанол.
В этом случае СО2 вводят в реакцию с метаном и водяным паром над никелевым катализатором, приводящую к образованию дополнительного количества СО и Н2, которые затем взаимодействуют, давая метанол.
Процесс проводят при давлении 67 – 100 атм. И температуре 200 – 260оС на катализаторах на основе оксидов меди и цинка.
Синтез Фишера-Тропша
Каталитическое гидрирование оксида углерода (синтез Фишера-Тропша) для получения углеводородов, в частности парафинов, в основном нормального строения и олефинов, является гетерогенной реакцией. Проводится она преимущественно над кобальтовыми или над железными катализаторами с использованием возможно более чистых смесей оксида углерода и водорода. Оптимальные рабочие температуры синтеза различны для различных катализаторов.
Никелевые и кобальтовые катализаторы дают оптимальные результаты при 170-205, железные — при 200-325°С. Синтез на никелевых катализаторах ведется практически только при нормальном давлении, так как при повышенном давлении резко усиливается образование карбонилов.
На железном и кобальтовом катализаторах можно работать без образования карбонилов при давлениях до 20 атм.
Считается, что при синтезе по Фишеру-Тропшу на железных катализаторах оксид углерода гидрируется с образование метиленовой группа, которая затем полимеризуется. Оксид углерода конвертируется в углекислоту. При этом кислород оксида углерода связывается, образуя воду. Этим реакциям благоприятствуют более высокая температура синтеза на железных катализаторах и активность железа по отношению к реакции конверсии.
С технической точки зрения решающее значение при синтезе Фишера-Тропша имеют, во-первых, очень большая теплота реакции каталитического гидрирования оксида углерода и, во-вторых, необходимость очень точного соблюдения постоянной температуры синтеза. В противном случае значительно возрастает нежелательное образование метана. Кроме того, при высоких температурах наблюдается отложение углерода на катализаторе, приводящее к быстрой его дезактивации.
Производство синтетического газа, свойства и его значение
- Группа авторов Войти
Что такое открытый доступ?
Открытый доступ — это инициатива, направленная на то, чтобы сделать научные исследования бесплатными для всех.
Наши авторы и редакторы
Мы являемся сообществом из более чем 103 000 авторов и редакторов из 3 291 учреждения в 160 странах мира, включая лауреатов Нобелевской премии и некоторых самых цитируемых исследователей мира. Публикация на IntechOpen позволяет авторам получать цитирование и находить новых соавторов, а это означает, что больше людей увидят вашу работу не только из вашей собственной области исследования, но и из других смежных областей.
Оповещения о содержимом
Краткое введение в этот раздел, посвященный открытому доступу, особенно с точки зрения IntechOpen
Как это работаетУправление предпочтениями
Контакты
Хотите связаться? Свяжитесь с нашим головным офисом в Лондоне или командой по работе со СМИ здесь:
Карьера
Наша команда постоянно растет, поэтому мы всегда ищем умных людей, которые хотят помочь нам изменить мир научных публикаций.
Рецензируемая глава в открытом доступе
Автор:
Рагда Ахмед Эль-Нагар и Алаа Али ГанемПредставлено: 21 ноября 2018 г. Отредактировано: 27 августа 2019 г.Опубликовано: 27 ноября 2019 г.
DOI: 10.5772/intechopen.89379
Скачать бесплатноиз отредактированного тома
Отредактировано Chaouki Ghenai и Abrar Inayat
Подробности книги Заказ. 1872 загрузки глав
1872 загрузки глав
Посмотреть полные показатели
СКАЧАТЬ БЕСПЛАТНОРекламное объявление
Аннотация
Большое внимание уделяется сокращению использования нефтепродуктов в качестве топлива, поэтому синтетический газ (синтетический газ) открывает большие возможности для устойчивого развития энергетики. Синтез-газ создается либо газификацией растительной биомассы, либо пиролизом отходов (на основе углерода). В принципе синтез-газ можно производить из любого углеводородного сырья. В основном это влияет на процесс сгорания в двигателях внутреннего сгорания. Наиболее важным является предел воспламеняемости, который очень важен для безопасности, а также скорость ламинарного пламени или скорость горения, которая является важным параметром для исследования работы камеры сгорания и характеристик выбросов.
Keywords
- synthetic gas (syngas)
- petroleum products
- pyrolysis
- gasification
- thermo-chemical process
- partially combustion
- flammability
1. Introduction
The synthesis gas is defined as a gas с H 2 и CO в качестве основных компонентов топлива. Рядный синтез-газ также содержит в основном значительные количества CO 2 и H 2 O. Поскольку синтетический газ обычно используется при более высоких давлениях для синтеза химикатов и топлива (рис. 1), N 9Содержание 0077 2 обычно должно быть сведено к минимуму в синтетическом газе. Однако биосинтез-газ производится из биомассы и химически идентичен синтез-газу. Это определение соответствует определению конференции SYNBIOS.
Однако биосинтез-газ производится из биомассы и химически идентичен синтез-газу. Это определение соответствует определению конференции SYNBIOS.
Рисунок 1.
Текущий мировой рынок синтез-газа, всего ~6 ЭДж/год.
Сингаз химически отличается от газов, обычно образующихся в процессах газификации при низких температурах, включая реакторы с псевдоожиженным слоем [1]. Для ясности, газ, производимый такими реакторами, упоминается в этом отчете как «продуктовый газ». Продуктовый газ определяется как топливный газ с H 2 и CO, а также со значительными количествами углеводородов, таких как метан. Продуктовый газ содержит CO 2 и H 2 O, а часто и N 2 , что также неизбежно.
В химической промышленности синтетический газ является важным промежуточным продуктом. Каждый год в мире производится около 6 ЭДж синтез-газа, что составляет почти 2% от текущего мирового потребления первичной энергии. Аммиачная промышленность доминирует на мировом рынке синтез-газа (в основном из ископаемого топлива, такого как уголь, природный газ и нефть/остатки) [2]. Производство водорода для использования на нефтеперерабатывающих заводах, например, обработка водорода и метанола являются другими важными областями применения. Текущее распределение синтез-газа на рынке показано на рисунке 1.
Аммиачная промышленность доминирует на мировом рынке синтез-газа (в основном из ископаемого топлива, такого как уголь, природный газ и нефть/остатки) [2]. Производство водорода для использования на нефтеперерабатывающих заводах, например, обработка водорода и метанола являются другими важными областями применения. Текущее распределение синтез-газа на рынке показано на рисунке 1.
Реклама
2. Основные свойства синтез-газа
Различные характеристики синтез-газа могут влиять на процесс сгорания в двигателях внутреннего сгорания (ВС). Предел воспламеняемости синтез-газа является одним из наиболее важных свойств безопасности двигателя внутреннего сгорания и топлива. Кроме того, ламинарная скорость пламени [3] (скорость горения) является важным параметром для исследования работы камеры сгорания и характеристик ее выбросов.
2.1 Пределы воспламеняемости сингаза
Предел воспламеняемости обычно используется в качестве показателя воспламеняемости газа. Это описывает диапазон концентраций топлива в топливно-воздушной смеси при определенных температуре и давлении, которые позволяют воспламенению пламени распространяться и поддерживать пределы воспламеняемости [4], известные в соответствии с общепринятыми понятиями как топливно-воздушные смеси. зоны, в которых возможно распространение пламени и где огонь не может распространяться. В первую очередь влияет топливо, направление распространения, размер и форма камеры сгорания, температура и давление [4]. А для топливно-воздушной смеси существует два различных предела воспламеняемости, а именно: наименьшая граница топлива, через которую может распространяться пламя, называется нижней границей воспламеняемости (НВГ), а самая богатая называется верхней границей воспламеняемости (ВВП). Тот факт, что Н 2 и CO являются основными огнезащитными компонентами сингаза, унаследовавшего характеристики этих газов. Наличие в газовых смесях инертных газов, таких как азот и углекислый газ, снижает предел воспламеняемости.
Это описывает диапазон концентраций топлива в топливно-воздушной смеси при определенных температуре и давлении, которые позволяют воспламенению пламени распространяться и поддерживать пределы воспламеняемости [4], известные в соответствии с общепринятыми понятиями как топливно-воздушные смеси. зоны, в которых возможно распространение пламени и где огонь не может распространяться. В первую очередь влияет топливо, направление распространения, размер и форма камеры сгорания, температура и давление [4]. А для топливно-воздушной смеси существует два различных предела воспламеняемости, а именно: наименьшая граница топлива, через которую может распространяться пламя, называется нижней границей воспламеняемости (НВГ), а самая богатая называется верхней границей воспламеняемости (ВВП). Тот факт, что Н 2 и CO являются основными огнезащитными компонентами сингаза, унаследовавшего характеристики этих газов. Наличие в газовых смесях инертных газов, таких как азот и углекислый газ, снижает предел воспламеняемости.
2.2 Ламинарная скорость пламени
Ламинарная скорость вспышки – это скорость, с которой пламя распространяется в направлении поверхностей волн разрежения в условиях ламинарного течения через тихие немаркированные топливно-окислительные смеси [5]. Поскольку LFV очень чувствителен к работе камеры сгорания и характеристикам выбросов, он очень важен для исследования работы камеры сгорания. На это влияет состав топлива, коэффициент эквивалентности смеси, температура и давление.
2.3 Состав синтез-газа и его теплотворная способность
Состав газа производителя зависит от сырья, размера частиц, скорости потока газа и потока сырья, конфигурации химического реактора, рабочих условий или процесса газификации, газификатора и катализатора, а также времени пребывания газа . Но в основном на него влияет температура реактора, на которую, в свою очередь, влияет величина ЭР. Кроме того, концентрации CO, H 2 и CH 4 в генераторном газе также контролируются химическими реакциями в процессе газификации.
Таким образом, на теплотворную способность генераторного газа оказывает значительное влияние тип окислителя, используемого для газификации. По мере увеличения УЭС, а затем снижения концентрации этих полезных компонентов из-за интенсификации горения при более высоких значениях УЭС концентрации СО и Н 2 достигают максимального значения. С увеличением ЭВ увеличиваются концентрации CO 2 и N 2 в генерирующем газе [4]. Воздух в качестве окислителя производит синтетический газ с относительно высоким содержанием азота и, следовательно, с более низкой теплотворной способностью, которая обычно не превышает 6 МДж/Нм 3 .
Производственный газ относится к топливным газам низкого качества. Типичный состав газификации биомассы воздушного реактора с нисходящим потоком воздуха с окислителем следующий: 15–20 % H 2 , 15–20 % CO, 0,5–2 % CH 4 , 10–15 % СО 2 и остальные компоненты N 2 , O 2 и CXHY. Если концентрация компонентов топлива значительно повышена и газ называют средней теплотой сгорания, до 16 МДж/Нм 3 [6], где используется кислород или водяной пар или их смесь.
Если концентрация компонентов топлива значительно повышена и газ называют средней теплотой сгорания, до 16 МДж/Нм 3 [6], где используется кислород или водяной пар или их смесь.
Реклама
3. Производство синтез-газа
Синтез-газом или синтез-газом называется монооксид углерода (СО)-водород (H 2 )-содержащая газовая смесь. Углекислый газ (CO 2 ) и другие компоненты, такие как вода (H 2 O), также могут присутствовать в синтетическом газе.
Химический синтез может использоваться в качестве строительного блока во всех продуктах, обычно производимых из сырой нефти или природного газа. Бензин и дизельное топливо — это топлива, определения которых основаны не на химическом составе, а на их физических свойствах, таких как кипение и вскипание.
Октановое число бензина в двигателе внутреннего сгорания (ДВС) является эмпирическим и основано на его фактических характеристиках. Это означает, что, по крайней мере, низкосортное смешивание возможно, если синтетическое топливо соответствует характеристикам сырой нефти на основе бензина или дизельного топлива.
Это означает, что, по крайней мере, низкосортное смешивание возможно, если синтетическое топливо соответствует характеристикам сырой нефти на основе бензина или дизельного топлива.
3.1 Производство топлива и химикатов путем газификации биомассы/угля или риформинга природного газа
Сырье должно быть газифицировано, если вы начинаете с твердого сырья, такого как биомасса или уголь. Перед газификацией может потребоваться измельчение или измельчение сырья (обычно углерода). Крупность частиц зависит от типа газификации. Для большинства заводов по газификации биомассы в качестве следующего шага требуется сушка. Сушка интегрируется в корпус реактора газификатора некоторыми газификаторами [7].
После газификации продукт представляет собой газ, известный как генераторный газ, содержащий примеси, которые необходимо удалить. Перед синтезом производителю газа обычно также требуется соотношение от H 2 до CO. H 2 :CO Оба.
3.2 Газификация
Все сырьевые углеводородные ресурсы, такие как уголь, тяжелая нефть или горючая биомасса, могут быть газифицированы в виде синтез-газа. В газификаторе происходит несколько реакций, но общая реакция может быть описана уравнениями (1) и (2).
В газификаторе происходит несколько реакций, но общая реакция может быть описана уравнениями (1) и (2).
Биомасса+O2→CO+h3+CO2+h3O+Ch5 E1
Побочные продукты: смола, уголь, зола.
Условия реакции:
Реакция также может быть выражена как:
CaHbOcNd+O2/h3O/N2→CO+h3+CxHyOz+CO2+h3O+Nh4+N2 E2
Твердый углерод частично окисляется кислородом (O 2 ), воздухом, паром (H
Таблица 1.
Состав генераторного газа [8].
Рисунок 2.
w3.org/2001/XMLSchema-instance”> Газификатор [8].Это важный фактор в определении технического механизма и экономической целесообразности системы газификации. Эффективность газификации зависит от типа используемой биомассы, размера ее частиц, значения ER и конструкции реактора [8].
Эффективность газификации обычно определяется по низшей теплотворной способности. КПД рассчитывается как отношение общей энергии генераторного газа (физической и химической) к химической энергии исходного сырья (теплотворная способность). В зависимости от типа и конструкции газификатора, а также от характеристик топлива КПД механического газификатора может варьироваться от 60 до 75%. Полезное определение эффективности газификации (%), используемое для двигателей, выглядит следующим образом:
ηm=Hg×QgHs×Ms×100
где ηm – эффективность газификации (%) (механическая), Hg – теплотворная способность газа (кДж/м 3 ), Qg – объемный расход газа (m 3 /с), Hs – низшая теплота сгорания топлива газификатора (кДж/кг), Ms – расход твердого топлива газификатора (кг/с).
3.3 Выход синтез-газа
Выход синтез-газа измеряется массой произведенного в кубических метрах на массу сырья, подаваемого в систему Выход прямо пропорционален разнице в ЭС и времени пребывания газа в область редукции [9]. Содержание золы в биомассе также оказывает значительное влияние и ограничивает выход производителя газа.
3.4 Очистка и охлаждение генераторного газа
Горючий газ может использоваться в качестве сырья для производства химикатов, таких как метанол, или в двигателях внутреннего сгорания для прямого использования тепла.
Реклама
4. Производство дизельного топлива Фишера-Тропша
Одним из коммерчески доступных методов производства чистого синтетического топлива из синтетического газа является метод Фишера-Тропша. В промышленном отношении уголь/нефтяной кокс/биомасса выделяют огромное количество углекислого газа, который можно использовать для увеличения производства топлива.
Из-за повышенного уровня углекислого газа в атмосфере, а также истощения запасов традиционных видов топлива, научные исследования рекомендуют химическую переработку углекислого газа в возобновляемое топливо и дополнительные химикаты [8].
Производство синтетического топлива из синтез-газа является выгодным процессом благодаря его мобильности, а также большому количеству химической энергии, сэкономленной без дальнейшей обработки и простому в использовании.
Сырой синтез-газ подвергается множеству энергоемких процессов для выполнения стехиометрических требований (2,05 < H 2 /CO < 2,15) для Фишера-Тропша, включая удаление двуокиси углерода для последующего связывания, чтобы смягчить негативное воздействие выбросов двуокиси углерода. Абсорбционные методы с моно- и диэтиламинами являются наиболее популярными технологиями удаления углекислых газов из синтез-газа. Эти процедуры являются энергоемкими из-за промежуточных стадий абсорбции, десорбции и сжатия.
Основная реакция Фишера-Тропша заключается в получении алифатических длинноцепочечных насыщенных углеводородов из синтез-газа (уравнение (3)). Существует множество побочных реакций, протекающих на активных центрах, сопровождающих основную реакцию (уравнение (4)).
Исходная реакция ФТ:
nCO+2nh3→Ch3n+nh3O;Δh398K=−152 кДжмоль−1 E3
Углекислый газ также является отходом синтеза Фишера-Тропша и считается, что он влияет на целевой выход получаемых жидких углеводородов, а также присутствие углекислого газа может привести к существенному снижению активности каталитической реакции [10]. Это связано с реакцией конверсии водяного газа (WGS) (уравнение (4)), с помощью которой восполняется недостаток водорода и во время реакции выделяется большое количество диоксида углерода.
Реакция конверсии водяного газа:
CO+h3O⇌CO2+h3; Δh398K=-41,2 кДжмоль-1 E4
Сообщалось, что двуокись углерода, содержащаяся в синтетическом газе, играет роль окислителя на восстановленном Co/γ-Al 2 O 3 , что влияет на конверсию окиси углерода и селективность по углеводородам C5+. Другая роль двуокиси углерода была предложена в качестве инертного газа в катализаторах на основе кобальта [10]. Другой подход описывает образование диоксида во время реакции Фишера-Тропша, который будет уменьшаться при использовании синтез-газа, содержащего диоксид углерода, поскольку равновесие имеет тенденцию быть направленным в обратном направлении, не влияя на процесс Фишера-Тропша.
Изменение равновесия диоксида углерода является первым этапом Фишера-Тропша (уравнение (6)), что приводит к увеличению доли атомов кислорода в монооксиде углерода, который извлекается водой по сравнению с карбоновыми катализаторами на основе железа, содержащими синтетический газ. . Образующийся при этом монооксид углерода подвергается дальнейшей обработке по методу Фишера-Тропша.
Реакция Будуара:
2CO⇌CO2+Cs; Δh398K=-172,5 кДжмоль-1 E5
Модифицированный CO 2 -Реакция FT:
СО2+h3⇌CO→2nh3→Ch3n+nh3O+h3O E6
Прямой CO 2 гидрирование:
nCO2+2nh3→Cnh3nn=2–4+nh3O E7
Низкая селективность 10Co5Fe, нанесенного на катализатор из углеродных нановолокон, для образования метана в ходе реакции Фишера-Тропша. Повышение уровня углекислого газа в синтетическом газе дает только 22% углеводородов C5+.
Fe 3 O 4 катализирует превращение углекислого газа в монооксид углерода за счет обратного отклика системы вода-газ-сдвиг, а χ-Fe 5 C 2 занимается добычей углеводородов.
Каталитическая трансформация синтез-газа была продемонстрирована с использованием бифункционального Fe-Co, подкрепленного иерархическим HZSM-5, 16% (мол.%) диоксида углерода в условиях дефицита водорода. 1Fe:2Co (мас.%) — наиболее эффективная биметаллическая смесь нескольких комбинаций железа и кобальта.
Объявление
5. Заключение
Синтез-газ определяется как газ с H 2 и CO в качестве основных компонентов топлива.
Предел воспламеняемости синтез-газа и ламинарная скорость пламени являются основными свойствами синтез-газа.
Синтез-газ может быть получен путем газификации биомассы/угля или риформинга природного газа, а выход измеряется массой произведенного газа в кубических метрах на массу исходного сырья.
Метод Фишера-Тропша является одним из коммерчески доступных методов производства чистого синтетического топлива из синтез-газа.
Ссылки
- 1.
 Abdelkader A, Daly H, Saih Y, Morgan K, Mohamed MA, Halawy SA, et al. Паровая конверсия этанола на Co 3 O 4 -Fe 2 O 3 смешанные оксиды. Международный журнал водородной энергетики. 2013;38:8263-8275
Abdelkader A, Daly H, Saih Y, Morgan K, Mohamed MA, Halawy SA, et al. Паровая конверсия этанола на Co 3 O 4 -Fe 2 O 3 смешанные оксиды. Международный журнал водородной энергетики. 2013;38:8263-8275 - 2. Диас Х.А., Ахаван Х., Ромеро А., Гарсия-Мингиллан А.М., Ромеро Р., Жируар-Фендлер А. и др. Кобальт и железо, нанесенные на углеродные нановолокна, как катализаторы синтеза Фишера-Тропша. Технология переработки топлива. 2014;128:417-424
- 3. Эсмаили Э., Мостафави Э., Махинпей Н. Экономическая оценка комбинированного цикла комплексной газификации угля с улавливанием сорбента CO 2 . Прикладная энергия. 2016;169:341-352
- 4. Jiang F, Zhang M, Liu B, Xu Y, Liu X. Взгляд на влияние носителя и промотора калия или серы на синтез Фишера-Тропша на основе железа: понимание контроля каталитическая активность, селективность по отношению к низшим олефинам и дезактивация катализатора.
 Катализ Наука и технологии. 2017;7:1245-1265
Катализ Наука и технологии. 2017;7:1245-1265 - 5. Mandal S, Maity S, Gupta PK, Mahato A, Bhanja P, Sahu G. Синтез среднего дистиллята посредством низкотемпературной реакции Фишера-Тропша (LTFT) на мезопористых кобальтовых катализаторах, нанесенных на SDA, с использованием синтез-газа, эквивалентного газификации угля. Прикладной Катализ A: Общие. 2018;557:55-63
- 6. Шашанк Б., Анна М.В., Среедеви Ю. Использование углекислого газа, вызывающего парниковый эффект, для производства более чистого дизельного топлива Фишера-Тропша. Журнал чистого производства. 2019;228:1013-1024
- 7. Yu X, Zhang J, Wang X, Ma Q , Gao X, Xia X, et al. Синтез Фишера-Тропша на модифицированном метилом Fe 2 O 3 @SiO 2 катализаторы с низкой селективностью по CO 2 . Прикладной катализ B: экологический. 2018;232:420-428
- 8. Visconti CG, Martinelli M, Falbo L, Infantes-Molina A, Lietti L, Forzatti P, et al.
 CO 2 гидрирование до низших олефинов на объемном катализаторе Fe, промотированном калием, с большой площадью поверхности. Прикладной катализ B: экологический. 2017;200:530-542
CO 2 гидрирование до низших олефинов на объемном катализаторе Fe, промотированном калием, с большой площадью поверхности. Прикладной катализ B: экологический. 2017;200:530-542 - 9. Halder A, Kilianová M, Yang B, Tyo EC, Seifert S, Prucek R, et al. Высокоэффективный нанокатализатор оксида железа, декорированный медью, для CO 9 низкого давления.0077 2 преобразование. Прикладной катализ B: экологический. 2018;225:128-138
- 10. Кордули Э., Павелец Б., Кордулис К., Ликургиотис А., Фиерро Д.Л.Г. Гидродеоксигенация фенола на бифункциональных катализаторах на основе никеля: эффекты промотирования и поддержки Мо. Прикладной катализ B: экологический. 2018;238:147-160
Разделы
Информация об авторе
- 1. Введение
- 2. Основные свойства синтез-газа
- 3.
 Получение синтез-газа
Получение синтез-газа - 4. Fisher-Tropsch Diesel Production
- 5. Conclusion
Ссылки
Реклама
Написано
Raghda Ahmed El-Nagar и Alaa Ali Ghanem
. : 27 ноября 2019 г. СКАЧАТЬ БЕСПЛАТНО© 2019 Автор(ы). Лицензиат IntechOpen. Эта глава распространяется в соответствии с условиями лицензии Creative Commons Attribution 3.0, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
Химия – Syngaschem BV
В результате реакций образуется вода, что является преобладающим путем удаления атома O из CO. Железные катализаторы обладают активностью в отношении конверсии водяного газа (1), что означает, что образовавшийся продукт превращает воду в H 2 и CO 2 делают FTS на основе железа менее зависимыми от начального отношения H 2 :CO, которое может составлять всего 0,5: просто добавьте реакцию WGS (1) к символическому уравнению реакции FTS согласно одна молекула CO:
CO + 2H 2 = -CH 2 – + H 2 O (7)
что дает:
2CO + H 2 ⇋ -CH 2 – + CO 29003 FTS на основе Fe является предпочтительным вариантом для технологии преобразования угля в жидкость.
Adsorption and dissocation:
CO + * ⇋ CO ads (9)
CO ads + * ⇋ C ads + O ads (10)
H 2 + 2 * ⇋ 2 Ч объявлений (11)
O-rejection by water formation:
O ads + H ads ⇋ OH ads + * (12)
OH ads + H ads ⇋ H 2 O + 2 * (13)
C-Hydradation:
C ADS + H ADS ⇋ CH ADS + * (14)
CH ADS + H ADS . CH ADS + H ADS . CH . объявления + * (15)
CH 2,объявления + H объявления ⇋ CH 3, объявление + * (16)
Рост цепи:
CH 3, ADS + CH 2, ADS ⇋ C 2 H 5, ADS + * (17) H 5, ADS + * (17) 9007
2 H 5, ADS + * (17) 2 H 5, ADS + * (17) 9 2 H 5, ADS + * (17) 9
C 2 H 5, объявление ⇋ C 2 H 4 + H ADS (21) 7. 10078+ H . механизмы, например, в которых разрыву связи СО способствует реакция с водородом (рис. 3) [17-20] или рост цепи происходит за счет включения СО, также доступны в литературе и являются предметом интенсивных дискуссий.
10078+ H . механизмы, например, в которых разрыву связи СО способствует реакция с водородом (рис. 3) [17-20] или рост цепи происходит за счет включения СО, также доступны в литературе и являются предметом интенсивных дискуссий.
Рис. 3 Молекулярное моделирование диссоциации CO на поверхности железа (100) (адаптировано из Elahifard et al. [20]).
Рис. 4. Распределение продуктов Фишера-Тропша по представляющим интерес углеводородным фракциям в зависимости от роста цепи , альфа. На вставке показаны несколько графиков Андерсона-Шульца-Флори в логарифмической форме.
Распределение углеводородных продуктов
Синтез Фишера-Тропша представляет собой процесс полимеризации. Даже не зная точного механизма, мы можем выразить избирательность по отношению к продукту с помощью n атомов углерода как
, где C означает концентрацию углеводорода с n атомами углерода, а α – вероятность роста цепи.
Это распределение Андерсона-Флори-Шульца, см. рис. 4, где показано, как распределение произведения Фишера-Тропша зависит от вероятности роста цепи, α. Преобразование его в логарифмическую форму дает простую возможность проверить, соответствует ли измеренная картина селективности этому распределению:
, если построить график зависимости ln (S n /n) от n, см. вставку на рис. 4. чем предсказывалось, и также обычно наблюдается более высокая вероятность роста цепи для более длинных углеводородов, чем для более коротких [21].
Технология Фишера-Тропша На рис. 5 показаны различные типы реакторов, которые используются в настоящее время, а также условия процесса. Низкотемпературная FTS хороша для длинных цепей, парафинов, а высокотемпературная – для более коротких продуктов, т.е. если желаемым продуктом являются химикаты и/или бензин [22-25]. Реакторы LTFT представляют собой трехфазные системы с твердыми катализаторами, газообразными реагентами и газообразными и жидкими продуктами. LT и MTFT составляют основу современных установок GTL и CTL. Затем парафин подвергается гидрокрекингу с образованием в основном дизельного топлива и небольшого количества лигроина.
LT и MTFT составляют основу современных установок GTL и CTL. Затем парафин подвергается гидрокрекингу с образованием в основном дизельного топлива и небольшого количества лигроина.
В процессах LTFT на установках CTL и GTL можно использовать как железные, так и кобальтовые катализаторы [15,23,26]. Катализаторы LTFT на основе железа содержат промоторы, такие как калий и медь, а также структурный модификатор, такой как диоксид кремния. Эти катализаторы обычно готовят путем совместного осаждения элементов железа и меди с последующей пропиткой калием и структурными активаторами. После этого катализатору необходимо придать форму для использования либо в реакторе с неподвижным слоем (например, экструдаты), либо в суспензионном реакторе ФТ (например, высушенные распылением сферы) с последующим прокаливанием. Перед использованием в процессе ФТ окисленные железные катализаторы необходимо активировать или кондиционировать в водороде или синтез-газе.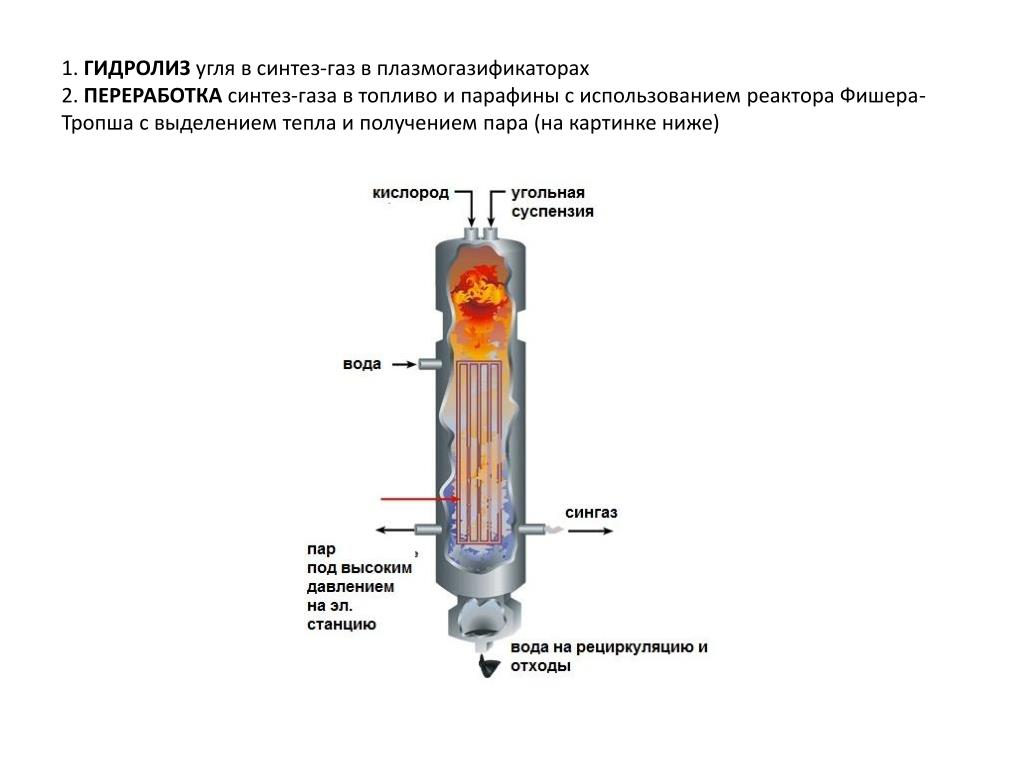 Во время процесса ФТ металлическое железо превращается в карбид железа и, в зависимости от условий, снова окисляется до оксида железа [27,28].
Во время процесса ФТ металлическое железо превращается в карбид железа и, в зависимости от условий, снова окисляется до оксида железа [27,28].
Рисунок 5. Обзор технологий Фишера-Тропша и используемых типов реакторов.
Перспективы Синтез Фишера-Тропша представляет собой проверенную технологию преобразования газа и угля в синтетическое топливо уже 90 лет назад [29,30]. В последнее время интерес к ней возник в связи с преобразованием солнечной и ветровой электроэнергии в синтетическое топливо и химикаты (Power to X). Хотя большая часть научных исследований сосредоточена на технологии GTL и кобальтовых катализаторах, именно технология CTL, основанная на железных катализаторах, получила наибольший рост в Китае. Были реализованы значительные улучшения катализаторов на основе железа, но улучшения стабильности и контроля над селективностью по-прежнему приветствуются. На самом деле, научное понимание сложных фаз железо-углерод-кислород в том виде, в каком они присутствуют в процессе, и взаимосвязи между составом катализатора и химией поверхности до сих пор не продвинулось далеко за пределы понимания очень упрощенных систем. В этом отношении металлический кобальтовый катализатор FTS изучен значительно лучше. Однако мы твердо убеждены в том, что детальное механистическое понимание химии Фишера-Тропша на основе железа крайне необходимо для создания рациональной основы для улучшения процесса.
В этом отношении металлический кобальтовый катализатор FTS изучен значительно лучше. Однако мы твердо убеждены в том, что детальное механистическое понимание химии Фишера-Тропша на основе железа крайне необходимо для создания рациональной основы для улучшения процесса.
См. также:
- van de Loosdrecht et al., Синтез Фишера-Тропша: катализаторы и химия в комплексной неорганической химии II (Elsevier, Amsterdam , 2013), 525-557. doi:10.1016/B978-0-08-097774-4.00729-4
- Сюй, Дж ян .; Ян, Y онг .; Li, Y ong -W ang; Недавние разработки в области преобразования угля в экологически чистое топливо в Китае. Топливо 2015, 152, 122-130.
- Роструп-Нильсен, Л. Дж. Кристиансен, Концепции производства синтез-газа, Серия каталитических исследований – Том. 10, Imperial College Press, Лондон, 2011 г.
 .
. - Л. Тримм, Образование кокса и его минимизация во время реакций парового риформинга, Catalysis Today, 37 (1997) 233-238.
- С. Бенгаард, Дж.К. Норсков, Дж. Сехестед, Б.С. Клаузен, Л.П. Нильсен, А.М. Моленбрук, Дж. Р. Роструп-Нильсен, Паровой риформинг и образование графита на никелевых катализаторах, Journal of Catalysis, 209.(2002) 365-384.
- В. тер Хаар, Дж. Э. Фогель, в: Proceedings of the Sixth World Petroleum Congress, Frankfurt am Main, Germany, 1963.
- С. Бхарадвадж, Л.Д. Шмидт, Каталитическое парциальное окисление природного газа в синтетический газ, Технология обработки топлива, 42 (1995) 109-127.
- H. Hu, E. Ruckenstein, Каталитическая конверсия метана в синтез-газ путем частичного окисления и риформинга CO2, Advances in Catalysis, Vol 48, 48 (2004) 297-345.
- Сенти, С. Ператонер, Возможности и перспективы химической переработки углекислого газа в топливо, Catalysis Today, 148 (2009 г.).) 191-205.
- С. Ньюсом, Реакция конверсии водяного газа, Catalysis Reviews-Science and Engineering, 21 (1980) 275-318.

- Н. Армор, Многочисленные роли катализа в производстве H-2, Applied Catalysis a-General, 176 (1999) 159-176.
- К. Чинчен, П.Дж. Денни, Дж.Р. Дженнингс, М.С. Спенсер, К.С. Во, Синтез метанола, 1. Катализаторы и кинетика, Applied Catalysis, 36 (1988) 1-65
- Klier, Синтез метанола, Advances in Catalysis, 31 (1982) 243-313.
- Сторч, Н. Голумбик, Р. Б. Андерсон, Фишер-Тропш и родственные синтезы, Wiley, New York, 1951.
- Иглесиа, С.К. Рейес, Р.Дж. Мадон, С.Л. Солед, Контроль селективности и дизайн катализатора в синтезе Фишера-Тропша – сайты, гранулы и реакторы, достижения в области катализа, 39 (1993) 221-302.
- П. ван дер Лаан, A.A.C.M. Бинакерс, Кинетика и селективность синтеза Фишера-Тропша: обзор литературы, Catalysis Reviews-Science and Engineering, 41 (19).99) 255-318.
- P. Steynberg, ME Dry, Fischer-Tropsch Technology, Studies in Surface Science and Catalysis, Vol. 152, Эльзевир, Амстердам, 2004
- E. Dry, J.
 C. Hoogendoorn, Технология процесса Фишера-Тропша, Catalysis Reviews-Science and Engineering, 23 (1981) 265-278.
C. Hoogendoorn, Технология процесса Фишера-Тропша, Catalysis Reviews-Science and Engineering, 23 (1981) 265-278. - Билоэн, В.М.Х. Сахтлер, Механизм синтеза углеводородов на катализаторах Фишера-Тропша, Успехи в области катализа, 30 (1981) 165-216.
- Р. Индервильди, С.Дж. Дженкинс, Д.А. Кинг, Новый взгляд на механизм Фишера-Тропша: Альтернативные пути производства высших углеводородов из синтез-газа, Journal of Physical Chemistry C, 112 (2008) 1305-1307
- Охеда, Р. Набар, А.Ю. Нилекар, А. Исикава, М. Маврикакис, Э. Иглесиа, Пути активации CO и механизм синтеза Фишера-Тропша, Journal of Catalysis, 272 (2010) 287-297.
- Р. Элахифард, М. Перес-Хигато, Дж.В. Niemantsverdriet, Прямая диссоциация CO на поверхности Fe(100) по сравнению с водородной диссоциацией: исследование DFT, Chem Phys Chem 13 (2012) 89-91.
- Дж. Доннелли, И.К. Йейтс, К.Н. Саттерфилд, Анализ и прогнозирование распределения продуктов синтеза Фишера-Тропша, Энергия и топливо, 2 (1988) 734-739.

- P. Steynberg, R.L. Espinoza, B. Jager, A.C. Vosloo, Высокотемпературный синтез Фишера-Тропша в коммерческой практике, Applied Catalysis a-General, 186 (1999) 41-54.
- Л. Эспиноза, А.П. Стейнберг, Б. Джагер, А.С. Вослу, Низкотемпературный синтез Фишера-Тропша с точки зрения Sasol, Applied Catalysis a-General, 186 (1999) 13-26.
- Дж. К. Герлингс, Дж. Х. Уилсон, Г.Дж. Крамер, Х. Куйперс, А. Хук, Х.М. Хьюисман, Технология Фишера-Тропша – от активного центра к коммерческому процессу, Applied Catalysis a-General, 186 (1999) 27-40.
- Т. Си, Разработка процессов и масштабирование: IV. История развития процесса синтеза Фишера-Тропша, Reviews in Chemical Engineering, 14 (1998) 109-157.
- Х. Дэвис, Синтез Фишера-Тропша: взаимосвязь между составом железного катализатора и технологическими параметрами, Catalysis Today, 84 (2003) 83-98.
- В. Нимантсвердриет, А.М. Ван дер Краан, В.Л. Ван Дейк, Х.С. Ван дер Баан, Поведение металлических железных катализаторов во время синтеза Фишера-Тропша, изученное с помощью мессбауэровской спектроскопии, рентгеновской дифракции, определения содержания углерода и измерения кинетики реакции, Journal of Physical Chemistry, 84 (19)80) 3363-3370.


 Abdelkader A, Daly H, Saih Y, Morgan K, Mohamed MA, Halawy SA, et al. Паровая конверсия этанола на Co 3 O 4 -Fe 2 O 3 смешанные оксиды. Международный журнал водородной энергетики. 2013;38:8263-8275
Abdelkader A, Daly H, Saih Y, Morgan K, Mohamed MA, Halawy SA, et al. Паровая конверсия этанола на Co 3 O 4 -Fe 2 O 3 смешанные оксиды. Международный журнал водородной энергетики. 2013;38:8263-8275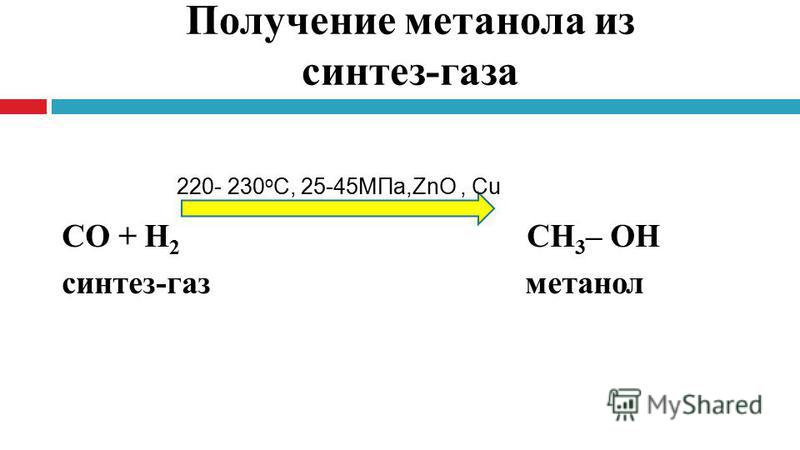 Катализ Наука и технологии. 2017;7:1245-1265
Катализ Наука и технологии. 2017;7:1245-1265 CO 2 гидрирование до низших олефинов на объемном катализаторе Fe, промотированном калием, с большой площадью поверхности. Прикладной катализ B: экологический. 2017;200:530-542
CO 2 гидрирование до низших олефинов на объемном катализаторе Fe, промотированном калием, с большой площадью поверхности. Прикладной катализ B: экологический. 2017;200:530-542 Получение синтез-газа
Получение синтез-газа
 C. Hoogendoorn, Технология процесса Фишера-Тропша, Catalysis Reviews-Science and Engineering, 23 (1981) 265-278.
C. Hoogendoorn, Технология процесса Фишера-Тропша, Catalysis Reviews-Science and Engineering, 23 (1981) 265-278.

Добавить комментарий